داروسازی لرستان
انرژی کشسانی
تعریف انرژی کشسانی : انرژی پتانسیل مکانیکی است که در ماده یا یک سامانه فیزیکی ذخیره می شود و برابر با کاری است که باید انجام شود تا تا در آن تغییر حجم یا شکل ایجاد کند . به عنوان مثال هنگامی که یک فنر را در آن تغییر شکل می دهیم یعنی آن را فشرده یا کشیده می کنیم نیرویی برابر با F=KXبه آن وارد می کنیم که در F نیرویی است که از طرف خارج می شود و واحد آن نیوتون است K ثابت فنر است واحد آن نیوتون بر متر است و X تغییر اندازه فنر است واحد آن متر است .دانش مکانیک جامدات گسترش یافته تا بتواند مکانیک اجسام صلب و ماده را پردازش کند و درک درستی از آن به دست آورد . انرژی پتانسیل کشسانی در به دست آوردن وضعیت تعادل مکانیکی کاربرد دارد . این انرژی در ماده ذخیره می شود یا به بیان دیگر پتانسیل است و می تواند به صورت دیگر انرژی یعنی انرژی جنبشی تبدیل می شود معادل ریاضی این انرژی به صورت زیر استU=1/2K(X2-X1)(X2-X1) ( 2)
در حالت کشسانی , برگشت پذیری یک اصل است به عبارت دیگر هنگامی که نیرویی به یک جسم وارد می شود و در ان انرژی پتانسیل کشسانی ذخیره می شود , پس ازبرداشتن آن نیرو , جسم حتما باید به حالت نخستینش بازگردد . هر ماده ای دارای درجه محدودی از شکل پذیری است و بیش از آن ممکن است دچار گسیختگی یا تغییر شکل های همیشگی شود . اگر از مرز کشسانی ماده رد شویم , آن ماده دیکر نمی تواند انرژی کشسانی را در خود نگه می دارد . برای دریافت میزان کشسانی بودن ماده باید وارد بحث های کرنش شد
مثال : هنگامی که یک چوب تر را در اثر نیروی وارد شده از خارج خم می کنیم این کاری که ما انجام دادیم مطابق فرمول 2 در آن به صورت انرژی پتانسیل کشسانی ذخیره می شود تا حدی از این قانون پیروی می شود ولی از آن حد به بعد اگر ما نیروی خارجی را زیاد کنیم چوب دیگر توانایی برگشتن به حالت اولیه را ندارد و برای همیشه شکسته باقی می ماند
انرژی کشسانی یک ماده یا میان میاده یک انرژی استاتیک در اندام ماده است و به تغییر فاصله میان اتم ها ربط دارد . انرژِ گرمایی به توزیع تصادفی انرژی جنتبشی در میان ماده ربط دارد و باعث نوسان های درونی ماده نسبت به حالت تعادلش می شود . برای نمونه گاهی وقتی یک جسم جامد زیر خمش , پیچش یا دیگر تغییر شکل ها قرار می گیرد در آن انرژی گرمایی ایجاد می شود و دمایش بالا می رود
انرژی پتانسیل کشسانی در سامانه های مکانیکی
اجزای یک سامانه مکانیکی اگر در برابر یک نیروی خارجی خود از تغییر شکلنشان دهد می تواند انرژی کشسانی را در خود ذخیره کند . این نیرو بسته به میزان تغییر شکلی که ایجاد کرده در جسم کار انجام داده که برابر با ضرب داخلی نیرو در جابجایی است . شناخته شده ترین نمونه در بحث انرژی کشسانی , فنر است . با توجه به قانون هوک یک ثابت برای فنر به اسم K تعریف می شود که به هندسه, سطح مقطع , جنس ماده و ... بستگی دارد. در یک بازه محدودی از تغییر شکل ها , K می ماند
K=-Fr/L-L0
در رابطه بالا L طول ثانویه یا تغییر شکل یافته فنر است به همین دلیل L می تواند از L0 بزرگتر باشد . مقدار Fr حتما باید به صورت برذاری و با علامتش نوشته شود . اگر L>L0 باشد نیروی منفی و اگر L
( L – L0 )__> X
قانون هوک به صورت زیر نوشت می شود:
Fr = - k x.
اگر تغییر شکل های بسیار کوچک در فنر را dx نیروی وارده را Kx بنامیم حال کل انرزی ذخیره شده در فنر ازتغییر شکل صفر تا طول نهایی L به صورت زیر بدست می اید:
U = {
در حالت کلی انرزی کشسانی در یکای حجم به صورت تابعی از تانسور کرنش نوشته می شود:
در این رابطه و ضریب های کشسانی لامه اند. رابطه ی میان تانسور تنش و کرنش به صورت زیر است :
برای مواردی که از مدل یانگ پیروی میکنند Y(همان مدول کشسانی ) سطح مقطع A , طول نخست L که به اندازه تغییر می کند :
در این رابطه Ue همان انرزی پتانسیل کشسانی است.
انرزی پتانسیل کشسانیدریکای حجم ماده برابر است با:
که در آن کرنش در ماده است.
گرد آورندگان: آقایان ناصر صید بگیان , محمد شفیعی , محمد جواد منتی , محسن امیری امرائی و سید احسان یعقوبی
اثرات زیست محیطی اشعه ایکس
همواره این امکان وجود دارد که به هر دلیلی یکی از الکترون های موجود در اتم از لایه
مربوطه جدا شود. چنانچه این الکترون از میدان کولنی هسته کاملاً خارج شود، می گوییم اتم
یونیزه شده است، که در این حالت یک یون مثبت و یک الکترون آزاد خواهیم داشت.
چنانچه الکترون جدا شده از لایه، کماکان در میدان کولنی هسته باقی بماند در این صورت
فقط یک جابجایی الکترون با کسب انرژی از لایه پایین تر به لایه بالاتر انجام شده است که
الکترون بلافاصله با آزاد نمودن آن انرژی به لایه خود باز می گردد. در این حالت میگوییم که
اتم برانگیخته و یا تهییج شده است. طبیعی است بیشترین انتقال انرژی به ماده از طریق
یونش خواهد بود
پرتوهای یونساز:
به پرتوهایی اطلاق می شود که هنگام عبور از ماده قادر به یونسازی در اتم های آن ماده
میباشند کمیسیون بین المللی یکاها و اندازه گیری پرتوها رااز نظر ساز و کار برخورد به دو
دسته تقسیم بندی کرده است
پرتو های مستقیم یونساز: شامل ذرات باردار نظیر آلفا، بتا، پروتون و یون های سنگین .
پرتوهای غیر مستقیم یونساز: شامل پرتوهای ایکس، گاما و نوترون ..
اشعه ایکس:
اشعه ی ایکس یا پرتوهای رونتگن نوعی از امواج الکترومغناطیس با طول موج حدود 01
تا 01 آنگستروم است که دربلورشناسی و عکسبرداری از اعضای داخلی بدن و عکسبرداری از
درون اشیای جامد و به عنوان یکی از روش های تست غیرمخرب در تشخیص نقص های موجود
در اشیای ساخته شده )مثلاً در لوله هاو…( کاربرد دارد .
پرتوهای ایکس را بوسیله بمباران هدفی فلزی با باریکه ای از الکترونهای سریع تولید می کنند.
قطعات اصلی لامپ اشعه ایکس شامل کاتد برای گسیل الکترونها و آند به عنوان هدف می باشد،
که هر دو درون لامپ خلا جای گرفته اند .
در سال ۵۹۸۱ ، درخشش کوتاه صفحه فسفرسانسی که در گوشه ای از آزمایشگاه نیمه تاریک بررسی
اشعه کاتدیک قرار داشت، ذهن آماده و خلاق رنتگن که در آن زمان استاد فیزیک بود، متوجه
پرتوهای تازه ای نمود که از حباب شیشه ای لامپهای کاتودیک بیرون زده و بی آنکه به چشم دیده
شود به اطراف پراکنده می شوند .
آن چه مایه شگفتی رنتگن شده بود، نفوذ این پرتوها از دیواره شیشه ای لامپ به بیرون و تأثیر آن
روی صفحه فاوئورسانس در گوشه ای نسبتا دور از لامپ در آزمایشگاه بود. رنتگن به بررسیهای خود
درباره کشف تازه که آن پرتو ایکس نامید )بخاطر فروتنی( ، ادامه داد. بعدها این اشعه رنتگن
نامیده شد
تاریخچه
همان طور که ذکر شد پرتو ایکس در سال ۵۹۸۱ توسط ویلهلم کنراد رونتگن )رنتگن(، فیزیکدان
آلمان کشف شد و به دلیل ناشناخته بودن ماهیت آن، پرتو ایکس مجهول نامیده شد. او پی برد که
برخورد پرتوهای کاتدی بر جداره های لامپ خلاء، پرتوهایی نامرئی با قدرت نفوذ بسیار زیاد تولید
می کند که بر روی فیلم های عکاسی تأثیر می گذارند .
این پرتوها توانایی عبور از لایه های ضخیم مواد کدر، از جمله بافت های بدن انسان را داشتند .
نحوه تولید پرتو کاتدی به این صورت است که وقتی دو قطعه فلز کاتد)مثبت( و آند)منفی( که
حامل حداقل ۵۱۱۱۱ ولت برق باشند وارد یک محفظه شیشه ای بسته باشند آن وقت فشار هوای
درون آن محفظه را کاهش دهیم یک پرتو نامریی از قطب منفی به قطب مثبت می رود. که این
پرتو را می توان با موادی که خاصیت فسفرسانس دارند را در مقابل پرتو بگذاریم می توان آن را
دید.
این گمان که پرتوهای ایکس، امواج الکترومغناطیس با طول موج بسیار کوتاهند، به کمک یک
آزمایش پراش دوگانه که در سال ۵۸۱۱ توسط سی.گ.بارکلا انجام گرفت، تائید شد. اثبات قطعی
ماهیت موجی پرتو ایکس در سال ۵۸۵۱ به وسیله ی فون لاوه ارائه شد
انواع پرتو ایکس
پرتو ایکس تکفام (تک رنگ):پرتو ایکسی که فقط دارای یک طول موج خاص است را پرتو ایکس
تکفام مینامند استفاده از پرتوهای ایکس تکفام و با شدت مناسب ، در آنالیز عنصری کاربرد بسیار
دارد.
′
IsoRay’s Cesium-131
IsoRay’s Cesium-131 Isotope Produces Excellent Results in Treating Metastatic Brain Cancer as Published in the Journal of Neurosurgery
100% Local (Resection Cavity) Freedom From Progression With 19.3 Month Median Follow-Up
Richland, WA (August 5, 2014) – – IsoRay Inc. (NYSE MKT: ISR), a medical technology company and innovator in seed brachytherapy and medical radioisotope applications, today announced the publication of the first major peer reviewed study showing superior results using IsoRay’s Cesium-131 seeds in the treatment of metastatic brain cancer.
IsoRay CEO Dwight Babcock commented, “We are extremely excited to have growing evidence that Cesium-131 isotope seeds continue to perform so well against aggressive cancers throughout the body and specifically now metastatic brain cancer. We believe our marketing efforts will be enhanced by teaming up with medical industry thought leaders as they seek better solutions and outcomes for their patients. As we continue to develop our product offerings internally with support from industry leaders, our message is clear and the medical community is becoming increasingly aware of the innovative alternative our Cesium-131 products offer to cancer patients.”
Dr. A. Gabriella Wernicke, Radiation Oncologist, and Dr. Theodore H. Schwartz, Neurosurgeon, with Weill Cornell, were two of the co-authors of the publication, which stated: “The use of post resection permanent Cesium-131 brachytherapy resulted in no local recurrences and no radiation necrosis.” The study followed 24 patients enrolled between 2010 and 2012, with a median 19.3 month follow-up period. Each patient had stranded Cesium-131 seeds implanted at the resection of a brain metastasis. During the follow-up period, study participants had 100% local (resection cavity) freedom from progression (FFP) and 93.8% one-year regional FFP. While patients with metastatic brain cancer experience significant hazards to survival (overall one-year survival rate in this study was 50%), the excellent local control of the surgically removed and Cesium-131 treated brain tumor – along with the lack of significant complications and the improved quality of life compared to other radiation therapy approaches – represents an important step forward in
managing these difficult cases.
Babcock said, “Commercialization requires published studies, like this one, that are peer reviewed, providing patients and family members with new insights into technological advances being made to treat these dreaded diseases. Leaders in the medical arena recognize and rely on the reported results in such publications, providing a means to stay abreast of these new and powerful weapons now available in the battle against cancer. As with this latest publication on metastatic brain cancers, I believe Cesium-131 is now a proven solution that can meet patient needs.”
IsoRay’s various products, including Cesium-131 seeds, sutured seeds, stranded mesh and the GliaSite® radiation therapy system, give physicians the ability to directly place a specified dosage of radiation in areas where cancer is most likely to remain after completion of a tumor removal or by placing seeds within the prostate. The ability to precisely place a specified dose of radiation means there is less likelihood for damage to occur to healthy surrounding tissue compared to other alternative treatments. IsoRay’s cancer fighting products diminish the ability of the tumor to recur, resulting in important benefits for patients in longevity as well as quality of life.
IsoRay is the exclusive manufacturer of Cesium-131. The pioneering brachytherapy therapy is one of the most significant advances in internal radiation therapy in 20 years. Cesium-131 allows for the precise treatment of many different cancers because of its unrivaled blend of high energy and its 9.7 day half-life (its unequaled speed in giving off therapeutic radiation).
In addition to its CMS codes, Cesium-131 is FDA-cleared and holds a CE mark for international sales in seed form for the treatment of brain cancer, prostate cancer, lung cancer, ocular melanoma cancer, colorectal cancer, gynecologic cancer, head and neck cancer and other cancers throughout the body. The treatment can be deployed using several delivery methods including single seed applicators, implantable strands and seed sutured mesh. IsoRay also sells several new implantable devices, including the GliaSite® radiation therapy system.
Safe Harbor Statement
Statements in this news release about IsoRay’s future expectations, including: the advantages of our products and their delivery systems, whether IsoRay will be able to continue to expand its base beyond prostate cancer, whether sales of our products will continue at historic levels or increase, whether the use of our products will increase or continue, whether we will continue to receive support from industry leaders, whether awareness of our products in the medical community will continue or increase, whether future studies of treatment of various cancers using our products will have favorable results, and all other statements in this release, other than historical facts, are “forward-looking statements” within the meaning of the Private Securities Litigation Reform Act of 1995 (“PSLRA”). This statement is included for the express purpose of availing IsoRay, Inc. of the protections of the safe harbor provisions of the PSLRA. It is important to note that actual results and ultimate corporate actions could differ materially from those in such forward-looking statements based on such factors as physician acceptance, training and use of our products, our ability to successfully manufacture, market and sell our products, our ability to manufacture our products in sufficient quantities to meet demand within required delivery time periods while meeting our quality control standards, our ability to enforce our intellectual property rights, whether additional studies are released and support the conclusions of past studies, whether ongoing patient results with our products are favorable and in line with the conclusions of clinical studies and initial patient results, patient results achieved when our products are used for the treatment of cancers and malignant diseases beyond prostate, successful completion of future research and development activities, whether we, our distributors and our customers will successfully obtain and maintain all required regulatory approvals and licenses to market, sell and use our products in its various forms, continued compliance with ISO standards as audited by BSI, the success of our sales and marketing efforts, changes in reimbursement rates, changes in laws and regulations applicable to our products, and other risks detailed from time to time in IsoRay’s reports filed with the SEC.
Powered by:ladies Shokoofe Karimpour ,Fateme Moridi ,Maryam Shokri
فلوئورسانس
فلوروسانس
نورتابناکی
نورتابناکی یا فتولومینسانس (Photoluminescence) فرایندی است که طی آن ماده فوتون را جذب کرده و سپس بازتاب میدهد.
در این روش نحوه تحریک بلور جامد از طریق جذب فوتونی است. در تجربه دیده میشود که طول موج جذب و انتشار عملا کمی فرق دارند و انرژی انتشار به مراتب کمتر(فرکانس پایین تر)است. این انتقال فرکانسی اصطلاحا انتقال استوکس نیز نامیده میشود.
دید کلی
بسیاری از سیستمهای شیمیایی ، فوتولومینسانس هستند، یعنی این سیستمها میتوانند توسط تابش الکترومغناطیسی برانگیخته شوند و متعاقب آن ، تابشی یا با همان طول موج یا با طول موج دیگر ، مجددا نشر کنند. دو نوع از متداولترین وجوه فوتولومینسانس «فلوئورسانس» و «فسفرسانس» هستند.
.
فسفرسانس و فلوئورسانس
فسفرسانس و فلوئورسانس پدیده هایی هستند که در آن ها یک ماده خاص که به طور عام به آن فسفر گفته می شود پس از قرار گرفتن در مقابل نور مرئی یا غیر مرئی یا حرارت، تحریک شده و این انرژی را در خود ذخیره می کند و سپس آن را را به صورت طیفی از امواج مرئی در طول مدت زمانی منتشر می کند.
تفاوت آن ها در اختلاف زمانی بین این دو دریافت و تابش یا به عبارت دیگر دوام تابش است. در فسفرسانس تحریک طولانی تر و تشعشع طولانی تری داریم و در فلوئورسانس تحریک کوتاه تر و تشعشع کوتاه تری داریم.
در فلوئورسانس که نمونه آن نور مهتابی یا صفحه تلویزیون است تابش آنی است و تقریبا بلافاصله بعد از قطع نور تمام می شود. در حالی که در فسفرسانس ماده بعد از قطع نور نیز تا مدتی به تابش ادامه می دهد که مقدار مدت آن بسته به ماده مورد استفاده می تواند از چند ثانیه تا چندین روز طول بکشد.
(نظریه فلوئورسانس
مثالهایی از رفتار فلوئورسانس را میتوان در سیستم های ساده و همچنین در سیستم های پیچیده شیمیایی ، در حالت گازی ، مایع و جامد مشاهده کرد. سادهترین نوع فلوئورسانس ، توسط بخارات اتمی رقیق به نمایش گذارده میشود. بعنوان مثال ، الکترونهای ۳s اتمهای سدیم بخارشده ، میتوانند با جذب تابش ۵۸۹۵ و ۵۷۹۰ آنگستروم به حالت ۳p برانگیخته شوند. پس از سپری شدن بطور متوسط ۸-۱۰ ثانیه ، الکترونها به حالت عادی بر میگردند و در ضمن این عمل ، تابش با همان دو طول موج را در کلیه جهات منتشر میکنند.
این نوع فلوئورسانس که در آن تابش جذب شده بدون تغییر دوباره منتشر میشود ، به تابش رزونانسی یا فلوئورسانس رزونانسی مشهور است. در مورد مولکولها یا یونهای چند اتمی نیز تابش رزونانسی به وقوع میپیوندد. بعلاوه اینکه تابش مشخصه با طول موجهای طولانیتر نشر میشود. این پدیده به نام جابجایی استوکس معروف است.
تقریبا تمام سیستمهای فلوئورسانس که برای تجزیه مفیدند، ترکیبات پیچیده آلی هستند که حاوی یک یا چند گروه عاملی آروماتیک میباشند..
طیف فلوئورسانس سنجها
طیف فلوئورسانس سنجها ، بر دو نوعند: نوع اول یک صافی مناسب را برای محدود کردن تابش تحریک و یک تکفامساز شبکهای یا منشوری را برای مجزا کردن یک پیک نشری فلوئورسان بکار میگیرد. چندین طیف نورسنج تجارتی را با دستگاههای رابطی که امکان استفاده از آنها بدین منظور میسر میسازد، میتوان خریداری کرد. طیف فلوئورسانس سنجهای واقعی دستگاههایی اختصاصی هستند که مجهز به دو تکفام ساز میباشند. یکی از این تکفام سازها تابش تحریک را به یک نوار باریک محدود میسازد؛ تکفام ساز دیگر امکان مجزا کردن یک طول موج فلوئورسان بخصوص را فراهم میکند..
اجزا سازنده فلوئورسانس سنجها و طیف فلوئورسانس سنجها
منابع فسفرسانس و فلوئورسانس
در بیشتر کاربردها ، به منبعی نیاز است که نسبت به لامپهای تنگستن یا هیدروژن که در اندازهگیریهای جذبی مورد استفاده قرار میگیرند، دارای شدت بیشتری باشد. معمولا یک لامپ کمان جیوهای یا گزنونی بکار گرفته میشود.
صافیها و تکفام سازها
صافیهای تداخلی و جذبی هر دو ، در فلوئورسانس سنجها بکار برده شدهاند. بیشتر طیف فلوئورسانس سنجها به تکفام سازهای شبکهای مجهزند.
آشکارسازها
علامت فلوئورسان نوعی ، دارای شدت کمی است و بنابراین برای اندازه گیری آن به ضرایب تقویتی بزرگی نیاز داریم. در دستگاههای فلوئورسانس حساس ، از لولههای فوتو تکثیر کننده بعنوان آشکارساز در مقیاس وسیعی استفاده میشود.
سلولها و محفظههای سلولها
سلولهای استوانهای و مستطیلی ساخته شده از شیشه و سیلیس هر دو در اندازه گیریهای فلوئورسانس بکار گرفته میشوند. باید نهایت دقت در طرح محفظه سلول به عمل آید تا مقدار تابش پراکندهای که به آشکارساز میرسد، کم شود. برای این منظور ، اغلب تیغههایی در داخل محفظه گذاشته میشود.
.
گونههای تابناکی (لومینسانس) | |
نوع | نحوهٔ برانگیختگی |
نورتابناکی (فتولومینسانس) (فلورسانس – فسفرسانس – فلورسانس تاخیری) | جذب نور (فوتونها) |
پرتوتابناکی (رادیولومینسانس ) | تابشهای یوننده (پرتو ایکس – پرتو آلفا – پرتو بتا – پرتو گاما) |
کاتدتابناکی (کاتدلومینسانس) | پرتو کاتدی (پرتو الکترونی) |
برقتابناکی (الکترولومینسانس) | میدان الکتریکی |
گرماتابناکی (ترمولومینسانس) | گرم کردن پس از ذخیرهٔ انرژی اولیه |
شیمیتابناکی (کمولومینسانس) | فرآیندهای شیمیایی (مانند اکسایش) |
زیستتابناکی (بیولومینسانس) | فرآیندهای زیستشیمیایی |
تریبولومینسانس | نیروهای اصطکاکی و الکترواستاتیکی |
صوتتابناکی (سونولومینسانس) | امواج فراصوت |
گرد آورندگان: خانم ها فاطمه صادقی، نادیا غلامی، زهرا گلمرادی
گاما دردرمان
گاما دردرمان
مقدمه
گاما پرتویی الکترومغناطیسی با بسامد بالا و در نتیجه انرژی بالاست. کاربرد اشعه ی ایکس از گاما بیش تر است. اشعهٔ گاما پرتویی یونی و در نتیجه برای سلامتی مضر است. پرتو گاما بطور معمول در نتیجهٔ فروپاشی حالتهای انرژی بالای هستههای اتم تولید میشود، اما روشهای دیگری نیز برای تولید آن وجود دارد. پل ویلارد دانشمند فرانسوی در سال ۱۹۰۰ در حین مطالعهٔ رادیوم موفق به کشف اشعهٔ گاما شد طول موج پرتو گاما بسیار کوتاه بوده و از 01/0 تا 1 آنگستروم تغییر میکند. جرم آن در مقیاس اتمی صفر، سرعت آن برابر سرعت نور و بار الکتریکی آن صفر است. انرژی پرتو گاما از ۱۰ کیلو الکترون ولت تا ۱۰ مگا الکترون ولت تغییر میکند. برد پرتو گاما بسیار زیاد، مثلاً در هوا چندین متر میباشد. خاصیت ایجاد یونیزاسیون و برانگیختگی در پرتو گاما نیز وجود داشته ولی به مراتب کمتر از ذرات آلفا و بتا میباشد. مثلاً اگر قدرت یونیزاسیون متوسط پرتو گاما را یک فرض کنیم، قدرت یونیزاسیون متوسط ذره بتا ۱۰۰ و ذره آلفا ۱۰۴ خواهد بود. قدرت نفوذ این پرتو به مراتب بیشتر از ذرات بتا و آلفا است. طیف انرژی پرتو گاما، همانند ذرات آلفا تک انرژی است، یعنی تمام فوتونهای گامای حاصل از یک عنصر رادیواکتیو دارای انرژی یکسانی هستند. این پرتو از لحاظ انرژی شباهت بسیاری با پرتو ایکس دارد، ولی مهمترین تفاوت این پرتو با پرتو ایکس در این است که اولاً منشأ تولید پرتو ایکس یک واکنش اتمی است، در حالی که منشأ تولید پرتو گاما یک برهمکنش هستهای است و دوم اینکه طیف پرتو گاما نسبت به پرتو ایکس متمرکزتر میباشد.از آنجا که عناصر تولید کننده پرتو گاما، فراورده فرعی تجزیه اتمی بوده و یا جزء ضایعات اتمی محسوب میشوند، استفاده از پرتو مذکور جزء ارزانترین روشهای نگهداری مواد غذایی است.
گاما و سلامت
پرتوی گاما از دیوار و سنگ نیز عبور میکند. هر ۹ میلیمتر سرب یا هر ۲۵ متر هوا شدت تابش آن را نصف میکند. این پرتو نیز با توجه به فرکانس بسیار بالا، انرژی زیادی دارد که اگر به بدن انسان برخورد کند از ساختار سلولی آن عبور کرده و در مسیر حرکت خود باعث تخریب ماده دزوکسی ریبو نوکلوئیک اسید یا همان DNA شده و سرانجام زمینه را برای پیدایش انواع سرطانها، سندرمها ونقایص غیر قابل درمان دیگر فراهم میکند وحتی این نقایص به نسلهای آینده نیز منتقل خواهد شد. برای جلوگیری از نفوذ تابش گاما به حدود ۱۰ سانتیمتر دیوارهٔ سربی نیاز است.[
این اشعه مانند امواج رادیویی دارای برد بسیار زیادی میباشد، قدرت نفوذ و تخریب این اشعه بسیارزیاد است. یک لایه ۱۵سانتیمتری بتن یا یک لایه ۲۰ سانتیمتری خاک فقط نیمی از این اشعه را میگیرد و همان نیمی دیگر اثرات زیانبار خود را بر جای میگذارد
اخطار: تا حد ممکن از اشعهٔ گاما استفاده نکنید. زیرا ممکن است به سرطان منجر شود. حداقل درصورت اجبار از لباس مخصوص استفاده کنید
تاثیرپرتوی گاما بربدن انسان
در خصوص اثرات زیان بار پرتوها بر موجودات زنده گروهی این خطرات را بسیار کمتر از مقدار واقعی در نظر می گیرندوگروهی تلاش می کنند بسیار بیشتر از آنچه که هست آنرا برجسته کننداین نوع تفکرات بدلیل عدم شناخت از ماهیت و عوارض پرتوها و میزان پرتوی قابل تحمل توسط بافت ها می باشد
اثرات پرتوهای یونساز به دو دسته اثرات قطعی و اثرات احتمالی تقسیم بندی می شوند. همواره یک حدآستانه وجود دارد و هنگامیکه میزان دز دریافتی بالاتر از حد آستانه بافت باشد اثرات قطعی پدیدار می گردد و سبب از بین رفتن تعداد زیادی از سلولهای بافتی در نتیجه اختلال یا از بین رفتن عملکرد اندامهای آسیب دیده می شود.
هرچه میزان دز دریافتی بیشتر باشد اثرات قطعی بیشتر می شوداثرات احتمالی در تمام سطوح پرتوگیری اتفاق می افتد. یکی از این اثرات سرطان ها می باشند که معمولا چند سال بعد از پرتوگیری ممکن است آشکار شده یا هرگز آشکار نشود.با افزایش دز دریافتی احتمال اثرات آن افزایش می یابد.
بروز اثرات احتمالی پرتوگیریهابرای دز های کم مقدار در یک شخص بعید است ولی هرگاه صحبت از یک جمعیت می شود می تواند کسر کوچکی از یک جمعیت را تشکیل دهد.بنابراین هیچگونه سطح ایمنی دز برای پرتوگیری احتمالی وجود نداردو تنها می توان با کنترل دز دریافتی میزان خطر احتمالی را کاهش داد.
واحد دز دریافتی بافتها را می توان با سیورت یا میلی سیورت بررسی نمود. یک سیورت عبارت است از انرژی معادل یک ژول پرتوی خاص که به یک کیلوگرم بافت منتقل می شود.( یک ژول انرژی جذب شده توسط یک کیلوگرم بافت را یک سیورت و یک ژول انرژی جذب شده توسط یک کیلوگرم ماده را یک گری می نامند.)
میزان حد آستانه برخی از بافت ها بر اساس میلی سیورت عبارتند از
میزان حدآستانه پرتو | بافت | |
20 میلی سیورت | غدد تناسلی | |
12 میلی سیورت | مغز قرمز استخوان – روده بزرگ – ریه – معده | |
5 میلی سورت | مثانه – سینه – جگر – مری – تیروئید – سایر اعضا | |
1 میلی سیورت | پوست – سطح استخوان | |
از اثرات قطعی پرتوها می توان ملتهب شدن پوست – تغییرات خونی – آب مرواریدو...و از اثرات احتمالی می توان سرطان ها و تغییرات در ماده وراثتی سلول های جنسی نام بردحساسیت بافت ها نسبت به پرتوها رابطه مستقیمی با قدرت تقسیم آنها دارد بدین معنی که بافت هایی مانند سلولهای پوششی روده.مخاطی دستگاه گوارش که قدرت تکثیر بالایی دارندیا اندامهایی مانند تخمدان ها که مراحل تقسیم طولانی دارند حساسیت بیشتری نسبت به پرتوگیری دارندهمچنین زمان برخورد پرتو با سلول بسیار مهم است سلول ها در مرحله تقسیم حساسترند.
تأثیر پرتودهی بر اورگانیسم های زنده
ویروس ها : کوچک ترین موجودات زنده می باشند که تنها در داخل سلول های زنده علائم حیاتی نشان می دهند. پرتوتابی با دوز بالا می تواند موجب غیر فعال شدن ویروس ها شود. این میزان دوز در محیط های آبی حدود 30 کیلوگری و در محیط های خشک به 40 کیلوگری میرسد. عملا پرتوتابی محصولات کشاورزی در چنین محدوده ای امکان پذیر نبوده و موجب تخریب آن خواهد شد. بنابراین مناسب ترین راه آلودگی زدایی ویروسی در چنین مواردی کاربرد حرارت درمانی است.
باکتری ها: به طور معمول در همه مواد غذایی حضور داشته و کنترل آنها از مهمترین راه های حفظ و نگهداری محصولات کشاورزی محسوب میگردد. علاوه بر تخریب ماده غذایی، بعضی از باکتریها در مقادیر بالای حد مجاز قادرند سلامت مصرف کنندگان را به خطر اندازند. طبیعت ماده غذایی، نحوه آماده سازی و چگونگی انبارداری از عوامل موثر در رشد و گسترش باکتری ها می باشند.
ارگانیسم های مختلف حساسیت های گوناگونی به پرتو دارند و در نتیجه کشتن جمعیت مخلوطی از آن ها یکسان نخواهد بود. پرتوتابی سبب تغییر در فلور و الگوی رشد می شود، پس باید نحوه اثر این تغییرات در ارتباط با فساد محیط مورد بررسی های دقیق قرار گیرد تا از خطرات احتمالی غیر قابل پیش بینی برای مصرف کنندگان جلوگیری شود. ممکن است پرتودهی با هدف نابودی تمام جمعیت میکروارگانیسم ها انجام گیرد. چنین مواردی مناسب نگهداری محصولات کشاورزی برای مدت طولانی و بدون نیاز به کاهش درجه حرارت می باشد. این شیوه کاربرد پرتو را Radappertization می گویند، که تقریبا معادل با روش حرارت درمانی استریلیزاسیون است. در این رابطه، هدف اصلی کاهش احتمال زنده ماندن میکروارگانیسم به میزان کمتر از یک، در جمعیت اولیه 1012 می باشد.
قارچها: . حساسیت قارچها در مقابل پرتوتابی، قابل مقایسه با بعضی از باکتری های فاقد اسپور می باشد. البته بسته به نوع گونه، میزان حساسیت متغیر خواهد بود. دوز کشنده در مورد مخمرها تقریبا در محدوده 6/4 تا 20 کیلوگری بوده، در حالیکه دوز کشنده سایر قارچها 5/2 تا 6 کیلوگری می باشد
گاما در پزشکی و صنعت
.. با اینکه اشعهٔ گاما به میزان زیاد ممکن است برای بدن خطر ناک باشد، ولی گاه فایده بسیار دارد. از این اشعه میتوان برای درمان برخی بیماریهای سرطانی و نارحتیهای پوستی استفاده کرد. همچنین در فیزیوتراپی نیز از اشعهٔ گاما استفاده میشود. درمان به وسیلهٔ اشعه گاما را رادیوتراپی مینامند. در صنعت نیز از اشعهٔ گاما که از رادیم و کبالت رادیواکتیو با قدرت زیاد تابش میشوند، برای پیدا کردن حفرههای ریز و شکستگیهای قطعات فلزی استفاده میکنند. از مهمترین کاربردهای دیگر پرتو گاما در پزشکی میتوان به استریلیزاسیون تجهیزات پزشکی مانند سرنگ که قابل استریل شدن در دمای بالا نیستنداشاره کرد.
پرتودرمانی
است پرتودرمانی یا رادیوتراپی (به فرانسوی: Radiothérapie) یکی از مهمترین شاخههای فیزیک پزشکی. پرتودرمانی به درمان بیماری با استفاده از پرتوهای نافذ مانند پرتوهای ایکس و آلفا و بتا و گاما که یا از دستگاه تابیده میشوند یا از داروهای حاوی مواد نشاندارشده ساطع میشوند گویند.
پرتو درمانی استفاده از پرتوهای یونساز برای ازبین بردن یا کوچک کردن بافتهای سرطانی است. در این روش در اثر آسیب DNA، سلولهای ناحیه درمان (بافت هدف) تخریب و ادامه رشد و تقسیم غیر ممکن میشود. اگرچه پرتو علاوه بر سلولهای سرطانی به سلولهای سالم نیز آسیب میرساند ولی اکثر سلولهای سالم بهبودی خود را دوباره بدست میآورند. هدف از پرتو درمانی از بین بردن حداکثر سلولهای سرطانی با حداقل آسیب به بافتهای سالم است.
کاربرد اصلی پرتو درمانی در معالجه و یا تقلیل امراض سرطانی میباشد.
دیگر کاربردهای پرتودرمانی: از بین بردن سلولهای سرطانی و ضایعات ارگانهای مختلف، بازتوانی و بهبود اعضای بدن بیمار (همچون کبد کلیه پروستات)، پیشگیری گسترش ضایعات اعضا و کاهش علائم بیماری (همانند درد).
دستگاهها و ابزارهای مختلف و گوناگونی برای درمان و توانبخشی بیمار توسط مهندسان پزشک ساخته و در اختیار پزشکان قرار گرفتهاست. یکی از این دستگاههای مهم و پرکاربرد رادیوتراپی و یا پرتودرمانی میباشد. به بیانی دیگر پرتودرمانی، استفاده از اشعه پر انرژی (معمولاً اشعه X) به منظور از بین بردن سلولهای سرطانی و ضایعات ارگانهای مختلف میباشد. به طور کلی رادیوتراپی را به ۳ قسمت رادیوتراپی خارجی، رادیوتراپی داخلی (براکی تراپی) و رادیوتراپی سیستمیک تقسیم میکنند. سلولهای سرطانی در مقایسه با سلولهای سالم به رادیو تراپی حساسیت بیشتری نشان میدهند و در نتیجه تعداد بیشتری از آنها از بین خواهند رفت البته رادیو تراپی بر سلولهای سالم ناحیه درمان نیز تاثیر میگذارد اما آنها بر خلاف سلولهای سرطانی معمولاً بهبود یافته یا به سرعت خود را ترمیم میکنند. رادیوتراپی همچنان برای پیشگیری گسترش ضایعات اعضا و برای کاهش علائم بیماری (همانند درد) نیز به کار برده میشود. اصولاً در این دستگاهها برای شناسایی و مکان یابی تومور و بافت مورد نظر برای دریافت پرتو از انواع مختلف پرتونگاری استفاده میگردد که شاید بتوان مرسوم ترین آنها را پرتونگاری مقطعی تخمینی (CT)، تصاویر رزونانس مغناطیسی (MRI) و اخیراً پرتونگاری مقطعی نشر پوزیترون (PET) معرفی نمود. حال پس از شناسایی موقعیت بافت مورد نظر بایستی مرحله شبیه سازی را شروع نمود که بر اساس آن آناتومی بیمار برنامه ریزی میشود. استفاده از پرتو در درمان سرطان یک فرایند پیچیدهاست که در بر گیرنده متخصصان آموزش دیده و تعداد زیادی از عوامل به هم پیوستهاست. متخصصین رادیوتراپی انکولوژی، متخصصین فیزیک پزشکی، دزیمتریست و متخصصین رادیوتراپی سالها دنبال لوازم و ابزار که به این فرایند، بخصوص در موقعیت یابی تومور، برنامه درمانی، اجرای درمان، و تحقیق کمک کنند، میگشتند. دقت در رادیوتراپی بسیار مهم است زیرا نتایج بالینی و تجربی نشان میدهند که کنترل تومور و پاسخ نرمال بافت میتواند یک عامل مهم درمقدار (دز) پرتو افشانی باشد و بنابراین، تغییرات کوچک در دز درمانی میتواند منجر به نتایج بزرگی در پاسخ تومور و یا بافت نرمال شود. به علاوه، دزهای تجویز شده درمانی تومور معمولاً الزاماً به دزی که برای بافت نرمال قابل تحمل است نزدیک است. بنابراین برای درمان بهینه، دز پرتوافشانی باید با دقت بسیار بالا انجام شود. یک میزان ±۵٪ توسط کمیسیون بینالمللی سنجش و واحدهای پرتو افشانی (ICRU) پیشنهاد شدهاست.
نزدیک دو سوم از بیماران سرطانی در جریان مداوای خود از پرتودرمانی استفاده میکنند. در سال ۲۰۰۴، این تعداد در آمریکا به ۱ میلیون نفر رسید. در این میان، سرطان پروستات، سرطان ریه، و سرطان سینه ۵۶٪ معضلات را تشکیل میدادند
انواع پرتودرمانی
پرتودهی ممکن است توسط دستگاهی خارج از بدن ( رادیوتراپی خارجی ) و یا توسط منبع پرتو در داخل بدن ( رادیوتراپی داخلی ) و یا توسط مواد رادیواکتیو باز درداخل بدن انجام شود ( رادیوتراپی سیستمیک ) . نوع پرتودهی به نوع تومور ، تحمل بافت های سالم اطراف محل آن ، مسافتی که پرتو باید در داخل بدن طی کند همچنین به سلامت عمومی بیمار ، تاریخچه بیماری و اینکه آیا بیمار از روشهای دیگر درمان استفاده خواهد کرد یا نه و مجموعه ای عوامل دیگر بستگی دارد . دربیشتر بیماران از روش پرتودرمانی خارجی و در تعداری از بیماران از سه روش پرتو درمانی خارجی ، داخلی ، سیستمیک همراه با هم و یا جداگانه استفاده میشود.
رادیوتراپی خارجی: پرتودرمانی یا رادیوتراپی خارجی معمولاً در بیماران سرپایی مورد استفاده قرار می گیرد. در بیشتر این بیماران نیاز به بستری شدن در بیمارستان نیست رادیوتراپی خارجی برای درمان انواع سرطان شامل سرطان مثانه ، مغز ، پستان ، رکتوم ، پانکراس ، معده ، گردن رحم ، حنجره ، ریه ، پروستات و رحم استفاده میشود علاوه بر این رادیوتراپی خارجی ممکن است برای کاهش دردهای متاستاتیک و یا مشکلات دیگر ناشی از گسترش تومورها مورد استفاده قرار گیرد.
رادیوتراپی حین جراحی (Intraoperative Radiotherapy): این روش نوعی پرتو درمانی خارجی همراه با جراحی است. IIORT برای درمان تومورهای متمرکز که نمی توان آنها را به طور کامل خارج کرد و یا ریسک عود مجدد وجود دارد استفاده می¬شود. بعد از خارج کردن تمام یا بیشتر بافت تومورال یک دوز زیاد با انرژی بالا مستقیماً به محل تومور در حین جراحی داده میشود ( بافت های سالم اطراف بوسیله شیلدهای مخصوصی حفاظت میشوند ) . بیمار بعد از عمل جراحی در بیمارستان بستری میشود این روش ممکن است در درمان تومور های تیروئید ، gynecological , colorectal روده باریک و لوزالمعده ( پانکراس ) استفاده شود . این روش برای درمان برخی از انواع تومور های مغز و سارکومای لگن در بزرگسالان تحت بررسی است .
رادیوتراپی تطبیقی سه بعدی 3D Conformal Radiation Therapy : رادیوتراپی تطبیقی برخلاف طرح درمان های قدیمی سه بعدی است و از کامپیوتر برای هدف گیری دقیق تر تومور استفاده می شود . امروزه بیشتر متخصصین سرطان شناسی از این روش استفاده می کنند . تصاویر سه بعدی CT ، MRI ، PET ویا SPECT تهیه و به کمک نرمافزارهای مخصوص ، پرتوهایی که با شکل تومور مطابقت دارند طراحی میشود . چون در این تکنیک بافت سالم اطراف تومور به طور وسیع از تشعشع دور است از دوزهای بالاتر برای درمان تومور می توان استفاده کرد . استفاده از این روش در تومورهای Nasopharyngeal ، پروستات ریه ، کبد و تومور های مغزی نتایج بهتری در برداشته است .
IMRT) Therapy Intensity-Modulated Radiation) : در این روش که یک نوع رادیوتراپی تطبیقی سه بعدی جدید است معمولاً از پرتوهای x با شدتهای متفاوت برای انتقال دزهای متفاوت پرتو به نواحی کوچک بافت به طور همزمان استفاده می شود . در این تکنولوژی نیز دزهای بالا به تومور و دزهای کمتر به بافتهای سالم اطراف می رسد . در برخی تکنیکها بیمار دز روزانه بیشتری دریافت می کند و زمان کل درمان کاهش و موفقیت درمان بیشتر می شود . IMRT ممکن است عوارض جانبی درمان را کاهش دهد. پرتودهی در این روش بوسیله یک شتاب دهنده خطی مجهز به کولیماتور Multileaf انجام می شود(کولیماتور به شکل دادن دقیق پرتوها کمک می کند). با چرخش دستگاه به دور بدن بیمار پرتوها از بهترین زوایا وارد تومور می شوند . پرتو ها تا حد امکان به طور دقیق با شکل تومور تطبیق داده می شوند . چون دستگاه IMRT بسیار تخصصی است مراکز سرطان شناس به ندرت از این وسیله استفاده می کنند . این تکنولوژی جدید برای درمان تومورهای مغزی، سروگردن، حلق بینی، پستان، کبد، ریه، پروستات و رحم مورد استفاده قرار می گیرد . IMRT برای هر بیمار و یا هر نوع توموری مورد استفاده قرار نمیگیرد.
رادیوتراپی داخلی( Brachy Therapy ) : در این روش منبع تشعشع که در یک پوشش نگهدارنده کوچک پیچیده شده در داخل تومور و یا بسیار نزدیک به آن قرار میگیرد و Implant یا ماده کاشتنی نامیده می شود. مواد کاشتنی ممکن است در شکلهای مختلف مانند سیمهای کوچک ، تیوبهای پلاستیکی ( کاتترها ) ribbans ( رشته ای ) کپسول و یا به شکل دانه ای وجود داشته باشد . مواد کاشتنی مستقیماً در داخل بدن گذاشته میشوند . در رادیوتراپی داخلی ممکن است بیمار نیاز به بستری داشته باشد . رادیوتراپی داخلی معمولاً به یکی از روشهای زیر انجام میشود که هرکدام به طور جداگانه توضیح داده شده است . در هر سه روش از مواد کاشتنی سربسته استفاده میشود .
رادیوتراپی داخل نسجی (Interstitial Rediotherapy): در این روش ماده رادیواکتیو در داخل بافت یا نزدیک محل تومور قرار میگیرد . این روش در درمان تومور های سر و گردن ، پروستات ، گردن رحم (Cervix ) ، تخمدان ، پستان ، نواحی لگن و اطراف مقعد استفاده میشود . در رادیوتراپی خارجی پستان ممکن است یک دوز بیشتر ( Boost ) به روش داخل نسجی یا خارجی به بیمار داده شود .
رادیوتراپی داخل حفره ای (Therapy Intracavitary): در این روش منبع رادیواکتیو بوسیله یک اپلیکاتور در داخل بدن قرار میگیرد . این روش معمولاً در درمان تومورهای رحم استفاده می شود . محققان در حال مطالعه و بررسی انواع رادیوتراپی داخلی برای درمان دیگر سرطانها شامل پستان، Bronchial، گردنی، مثانه، دهانی، Tracheal ,Rectal، رحم و واژن هستند.
رادیوتراپی سیستمیک( پزشکی هسته ای ): در این روش از مواد رادیواکتیو مانند I131 Strontium89. به صورت خوراکی و یا تزریقی استفاده می شود . این روش درمانی گاهی اوقات برای درمان سرطان تیروئید و لنفوم غیر هوچکینی بزرگسالان استفاده میشود . محققان در حال بررسی موادی هستند که بتواند برای درمان دیگر انواع سرطان استفاده شود .
منابع انرژی در رادیوتراپی خارجی
منابع پرتودهی مورد استفاده در رادیوتراپی خارجی ممکن است شامل انواع زیر باشد :
اشعه گاما یا x : این پرتوها از نوع تشعشع الکترومغناطیس محسوب می شوند، ولی طریقه تولید آنها متفاوت است . پرتوهای x بوسیله دستگاهی به نام شتاب دهنده خطی تولید میشوند . پرتوهای با انرژی پایین در تخریب سلولهای سرطانی سطحی و پرتوهای با انرژی بالاتر در درمان تومورهای عمقی تر بکار میرود. پرتوهای x میتوانند یک ناحیه بزرگ را مورد تشعشع قرار دهند . پرتوهای گاما از رادیو ایزوتوپهایی مثل ایدیدیوم Ir و CO60 منتشر میشوند . هر عنصر در یک زمان خاص واپاشی و میزان متفاوتی از انرژی را آزاد میکند که بر نفوذ آن به داخل بدن مؤثر است . در واپاشی کبالت پرتوی گاما منتشر میشود که در درمان با knife Gamma نیز مورد استفاده قرار میگیرد.
تشعشعات ذره ای ( Particle beams ): دراین روش از ذرات هسته ای پر انرژی به جای فوتون استفاده می شود . این روش درمانی ، رادیوتراپی ذره ای یا تشعشع ذره ای نامیده می شود . تشعشعات ذره ای به وسیله شتاب دهنده های خطی، سنکروترن و سیکلوترون تولید می شود. ذرات شتابدار عبارتند از : الکترون که به وسیله تیوب اشعه X تولید میشود، نوترون ها که به وسیله عناصر رادیواکتیو و تجهیزات مخصوص تولید می شوند. یون های سنگین مثل پروتون ها، هلیوم و ذرات باردار کوچک یعنی مزون که به وسیله شتابدهنده و یک سیستم مغناطیسی تولید میشوند. برخلاف پرتوهای ایکس و گاما ، پرتوهای ذره ای قدرت نفوذ کم دارند . بنابراین از این پرتوها معمولاً برای درمان تومورهای سطحی یا زیر جلدی استفاده می شوند .
درمان با پرتوی پروتون ( Proton beam therapy ): در این روش از پرتوهای پروتونی استفاده می شود که انرژی خود را در یک ناحیه کوچک ( Bragg peak ) از دست می دهند. در این ناحیه دزهای بالا بر روی تومور با حداقل آسیب به بافت های نرمال متمرکز می شود . پروتون درمانی فعلاً در مراکز محدودی در ایالات متحده استفاده می شود . این شیوه برای درمان تومورهایی که عمل جراحی مشکل یا پر مخاطره است به کار می رود . تحقیقات کلینیکی برای استفاده از این روش در درمان ملانومای چشم ، Retinoblastoma ( یک نوع تومور چشمی که بیشتر در اطفال زیر 5 سال اتفاق می افتد ) سارکومای عضلات مخطط، برخی انواع تومورهای سر و گردن ، پروستات ، مغز و ریه در حال انجام است.
درمان با پرتوی کربن ( carbon beam therapy ): در این روش از پرتوهای یون های کربن استفاده می شود که انرژی خود را در یک ناحیه ی کوچک (Bragg peak ) همانند پروتون از دست می دهند، و حداقل آسیب به بافت های سالم را در پی خواهد داشت. به علت هزینه ی بالای شتاب دهنده های تولید کننده ی یون های کربن با سرعت بالا ، به کار گیری این روش درمانی با محدودیت زیادی روبرو است.
منابع انرژی مورد استفاده در پرتو درمانی داخلی
منابع تشعشع مورد استفاده در رادیوتراپی داخلی عبارتند از : ایزوتوپهای رادیواکتیو مانند (I131 ) و Sr89 ، فسفر ،palladium ، سزیم ، ایریدیوم ، فسفات یا کبالت ، منابع دیگری هم در دست بررسی هستند .
Stereo tactic radiosurgery & Stereo tactic Rodiotherapy : در روش اول از یک دوز بالا برای تخریب بافت تومورال در مغز استفاده می شود . سر بیمار در یک قالب مخصوص که به جمجمه متصل است قرار می گیرد . از قالب به منظور تابش به خط مستقیم به تومور سر بیمار استفاده می شود . تابش دقیقاً در ناحیه مورد نظر خواهد بود. این روش بافتهای اطراف تومور عموماً از آسیب در امان خواهند ماند . این شیوه به سه صورت انجام می گیرد : روش متداول استفاده از فوتون های با انرژی زیاد شتاب دهنده خطی که Linac -based stereo tactic RT نامیده می شود. در دومین روش از پرتوی گامای CO60 و در روش سوم از پرتوهای ذرات باردار سنگین مثل پروتونها و یونهای هلیوم Stereo tactic استفاده می شود . این روش اکثراً در درمان تومورهای کوچک خوش خیم یا بد خیم مغز مثل مننژیوما ، و تومور هیپوفیز همچنین در درمان بیماریهای دیگر مثل پارکینسون، صرع ، تومورهای متاستاتیک مغز ( تومورهایی که از قسمتهای دیگر بدن انتشار یافتهاند ) ، به صورت منفرد و یا همراه با رادیوتراپی تمام مغز مورد استفاده قرار می گیرند.
Stereo tactic Radiotherapy : در این روش از همان شیوه مورد استفاده در روش های قبل ولی با دوزهای پایین در تعداد جلسات متعدد استفاده می شود . دزهای کم و تعداد جلسات زیاد نتیجه را بهبود بخشیده ، عوارض اشعه را به حداقل می رساند. این روش برای درمان تومورهای مغزی با همان روشی که در قسمتهای دیگر بدن بکار می رود، استفاده می شود . در تحقیقات بالینی سودمندی این دو شیوه به صورت منفرد و یا همراه با دیگر روش های پرتو درمانی در حال بررسی است .
روشهای پرتودهی
روشهای مختلفی برای پرتودهی و انتقال اشعه با قدرت نفوذ متفاوت وجود دارد، علاوه براین تعدادی از روشهای پرتو دهی میتواند بطور دقیق و کنترل شده برای درمان ناحیه کوچکی از بافت بدون آسیب به بافت و اندامهای اطراف استفاده شود، در حالیکه برای درمان نواحی بزرگتر از انواع دیگر پرتو استفاده میشود. مثلاً در مواردی از دستگاههای بزرگی که اشعه x و گاهی اشعه گاما یا الکترون تولید میکنند استفاده میشود، بیمار را به دقت بر روی تخت درمان میخوابانند آنگاه دستگاه دقیقاً بالای منطقهٔ سرطانی تنظیم میشود
. عوارض جانبی پرتودرمانی
باعث سوختگی پوست می شود(مشابه آفتاب سوختگی). معمولاً در طول دوره رادیوتراپی استحمام مجاز نمیباشد. به طور کلی پرتودرمانی موجب ریزش مو نمیگردد ولی اگر پرتودهی در ناحیه سر باشد می تواند باعث ریزش موی سر گردد
.
پرتودرمانی نوین
در پرتو درمانی از شتابدهندههایی ویژه برای تولید الکترون جهت نفوذ به درون بدن بیمار استفاده میشود. از پرتوهای فوتونی پر انرژی نیز استفاده میشود.
برای نمونه میتوان از سیستمهای چاقوی گاما، سایبر نایف، لیناک و توموتراپی نام برد. اما گاهی نیز از تکنیکهای کاشت رادیو ایزوتوپ، همانند برکیتراپی نیز استفاده میگردد.
در روشهای پرتودرمانی نوین نیز از پرتوهای با انرژی بالا از پروتون یا نوترون نیز استفاده میگردد (که به آن پروتون درمانی
و درمان با گیراندازی نوترون بور گویند) و استفاده از یونهای سنگینتر نیز در مرحله تحقیقات است.
چاقوی گاما
چاقوی گاما یا همان گاما نایف در حقیقت یک چاقو نیست بلکه نام تجاری و ثبت شدۀ وسیله ایست برای اعمال اشعه گاما با شدت بالا که به صورت هدف گیری نقاط مشخصی از ضایعات به کار می رود. این اشعه گاما از ماده رادیو اکتیو کبالت ۶۰ منتشر می شود. در سوئد برای بیشتر از 20 سال است که مورد استفاده و توسعه قرار گرفته و همکنون در کشورهایی چون آمریکا موجود است. برای بیمارانی که دارای تومور مغزی خوش خیم و یا دارای رگهای غیر عادیِ غیر قابل جراحی (بدلیل عمیق و در دسترس نبودن و یا نزدیک بودن به نقاط حیاتی مغز) هستند، استفاده می شود.
این روش بصورت سر پایی است و نیازی به جراحی و بیهوشی ندارد و در حدود 2 تا 3 ساعت به طول می انجامد.
کبالت 60 چیست؟
کبالت 59 در طبیعت وجود دارد و فلزی پایدار است (رادیو اکتیو نیست). وقتی کبالت 59 در یک میدان نوترونی قرار بگیرد ، با دریافت یک نوترون به کبالت 60 تبدیل خواهد شد که ایزوتوپ همدیگرند. کبالت 60 که رادیو اکتیو است دارای نیمه عمر 5.27 سال است ، که با انتشار یک بتای منفی و پس از آن تولید اشعه گاما ، به عنصر پایدار نیکل 60 تبدیل می شود. در این واپاشی، کبالت 60 یک الکترون(بتای منفی) با انرژی 315kev و دو اشعه گاما با انرژی های 1.17Mev و 1.33Mev منتشر می کند.
یک گرم کبالت60 حدود 50کوری اکتیویته دارد. که این مقدار می تواند قدرت یونیزه کنندگیی حدود 0.5 sievert/min را برای بدن داشته باشد. دوزی معادل 4 تا 5 سیورت برای کل بدن، می تواند در طول 30 روز نصف انسانها را از بین ببرد. که می توان بوسیله یک گرم ، تنها در طول چند دقیقه به اثر ذکر شده رسید.
برخی کاربردهای اشعه گاما:
_ برای ردیابی واکنش های شیمیایی
_ منبعی رادیو اکتیو برای کارهای پرتوپزشکی
_ برای عکسبرداری های صنعتی
_ برای محاسبه قطر و کلفتی برخی اشیا
_ برای میکروب کشی مواد غذایی
_ بعنوان منبع رادیو اکتیو برای کارهای آزمایشگاهی
همچنین در ساخت بمب کبالت نیز به کار می رود.
چاقوی گاما چاقویی بدون قابلیت برش
برای افرادی که دارای تومور مغزی هستند ممکن است زندگی کسل کننده و رنج آور باشد. اما نعمت انقلاب در تکنولوژی ، معالجه برای بسیاری بیماران را امیدوار کننده تر و راحت تر و بدون درد تر ساخته است.
تکنولوژیی که به نام «چاقوی گاما» مشهور است _بر خلاف نام آن_ یک چاقو نیست بلکه وسیله ای شبیه کلاه خود است که بوسیله آن مغز بیمار ، پرتوهایی به شدت کانونی شده را از منبع رادیو اکتیو دریافت می کنند که تومور را مورد هدف قرار می دهد ولی به بافت های دیگر صدمه نمی زند. چاقوی گاما مزیت های زیادی به همراه دارد اما کاستی های آن باید برای پیشرفت بیشتر مورد توجه قرار گیرد. تعدادی از مزیت های چاقوی گاما عبارتند از :
_ عدم نیاز به تراشیدن موی سر یا جراحی و بخیه
_ بدون زخم و درد بودن
_ عدم نیاز به بیهوشی بطوریکه بعد از این درمان مریض می تواند به کارهای روزانه اش بپردازد
_ نداشتن دوره نقاهت و یا غیبت از کار و خانواده
همچنین موثر تر از عمل های جراحی مرسوم می باشد و برای بیماران سالخورده بسیار مناسب است.
خطر کمتر ، هزینه کمتر
در میان مزایای زیاد آن به صرفه جویی در هزینه ها ، بدلیل حضور و بستری کمتر بیمار در بیمارستان باید اشاره کرد. همچنین مریض از خطرات عفونت و خونریزی و واکنش های منفی بدن به بیهوشی، مصون است.
پس از آنکه تکنولوژی چاقوی گاما در دانشگاه بدست آمد ، بر روی 200 مریض برای درمان آنها آزمایش شد. روش چاقوی گاما حدود 3 ساعت طول می کشد که نیاز به یک گروه متخصص ، متشکل از ،حداقل ، متخصص مغز و اعصاب و فیزیکدان پرتو پزشک ، دارد.
در حالی که مریض بی تحرک دراز کشیده ، گروه متخصص ابتدا به عکس برداری (magnetic resonance imaging) MRI یا CT(Computed Tomography) از مغز او اقدام می کنند. بعد یک کلاه بزرگ که دارای 201 منفذ خروجی به طرف سر بیمار است ، بر سر بیمار قرار می گیرد. از این منفذها باریکه های بسیار دقیق اشعۀ گامای کبالت 60 (Co-60) به تومور می تابانند. پرتو های منتشره در یک کانون منسجم می شوند. نقطۀ کانونی باید در حدود اندازه تومور باشد. فیزیکدان پرتو پزشک و متخصص مغز و اعصاب کار را با تابش دهی ملایم آغاز می کنند تا در نهایت مکان دقیق تومور هدف گیری شود. این عمل که به دفعات انجام می گیرد «شوت» نام دارد. در ضمن مریض دریافت اشعه را احساس نمی کند.
دز تابشی بسته به عمق و اندازه و پیشرفت تومور ، متفاوت است تا برای بافت های اطراف تومور حداقل خطر را داشته باشد.
روش چاقوی گاما یک روش چند رشته ایست و همانگونه که گفته شد فیزیکدان پرتو پزشک و متخصص مغز و اعصاب با همکاری یکدیگر این کار را انجام می دهند.
نکته مهمی که باید در اینجا مورد توجه قرار گیرد اینست که پرتو افشانی ها نباید حرکت ، فکر ، حافظه و اعمال عادی مغز را دچار مشکل و خطر کند. به دلیل دقت بالای چاقوی گاما ، از آن می توان بر روی کودکان نیز استفاده کرد.
نقش کامپیوتر و تصویر برداری پیشرفته
در اصل تکنولوژی چاقوی گاما 50 سال پیش در سوئد اختراع شد اما به طور گسترده استفاده نشد، تا امروزه که با پیشرفت های سریع صورت گرفته در تصویر برداری و علم کامپیوتر ، به مرحلۀ استفاده وسیع رسیده است.
هر نوع بدخیم از تومورهای مغزی بوسیله چاقوی گاما قابل درمان نیست. به عنوان مثال ضایعات بزرگتر از 4cm را نمی توان درمان کرد.
همچنین چاقوی گاما به صورت موفقیت آمیز در از بین بردن درد های آزار دهنده ای که مربوط به تیک های عصبی دردناک است بکار می رود. و در درمان ناهنجاری های وریدی(arteriovenous malformations) موسوم به AVMs و اختلالات عصبی مغز مفید است. چاقوی گاما بطور وسیع برای تومورهای مغزی خوش خیم مثل التهاب اعصاب شنوایی(acoustic neuromas) که در آن اعصاب شنوایی و اعصاب صورت بیمار بوسیله تومور تحت تاثیر هم قرار گرفته اند استفاده می شود. که می تواند بهبودیی حدود 80% را به دنبال داشته باشد و حتی عوارض باقی مانده در چهرۀ ناشی از سکتۀ مغزی را به حدود صفر می رساند.
ایمنی آ ن چقدر است؟
به خاطر اهمیت هدف گیری دقیق توسط "شوت" ها ، هرگونه عملی که این دقت را تنزل دهد نا مطلوب خواهد بود. جایگذاری دقیق کلاه چاقوی گاما، دقت عکس MRI، محدودۀ بافت مورد هدفگیری ، تعداد شوت ها و شدت آنها و ... همگی دارای اهمیت زیادی می باشند. در حقیقت برای تمام رادیوتراپی ها مکان یابی دقیق هدف ، مهم است. تنها بوسیله پزشکان مجرب، تجهیزات پیشرفته و دانش به روز است که می توان از دقت آزمایش ها و درمان اطمینان داشت. چون در صورتی که پزشک و همکاران او بی تجربه باشند و یا سلامتی بیمار را در مرتبه اول قرار ندهند و یا اینکه تجهیزات درمان مناسب نباشند، می تواند نتیجه عکس را به دنبال داشته باشد ، چون هرگونه انحراف از هدف گیری صحیح می تواند به جای تخریب تومور ، به تخریب بافتهای دیگر مغز بینجامد که اثرات جبران ناپذیر و دائمی را در پی خواهد داشت.
عوارض جانبی؟
معدودی عوارض جانبی را می تواند در پی داشته باشد. مثل ؛ ریزش مو، حالت تهوع و سر درد.
با اینکه چاقوی گاما تحولی در تکنولوژی است، اما هنوز از درمان پیشرفته و قطعی مشکلات مغزی و عصبی فاصله دارد.
چاقوی گاما روشی جدید برای درمان صرع و پارکینسون و سردرد است. چیزی که قبل از این روش امکان آن وجود نداشته است. این روش آینده ای روشن را برای درمان نوید می دهد.
گرد آورنذگان:خانم ها زهرا نیکنام،نگار گودرزی،ریحانه شجاعی
رادیو دارو ها
رادیو دارو چیست؟
در یک تعریف ساده به هر دارویی که در ساختار آن یک رادیو ایزوتوپ موجود باشد رادیودارو گفته میشود، رادیوایزوتوپها در واقع عناصر ناپایداری هستند که با توجه به ساختار اتمیشان از خود پرتو (Radiation) منتشر میکنند. این پرتوها که شامل پرتوهای آلفا (α)، بتا (β) و گاما (γ) هستند دارای طول موج و سطح انرژی متفاوتی هستند و بر همین اساس میتوانند در فرآیندهای مختلف تشخیصی و درمانی به کار گرفته شوند. سودمندترین رادیو ایزوتوپها در پزشکی هستهای رادیوایزوتوپهای تابش کننده پرتو گاما هستند، زیرا پرتوهایی که از این مواد در درونِ بدن تابش میشوند را میتوان از بیرون بدن به سادگی تشخیص داد.
تاریخچه رادیو داروها:
اولين استفاده کلينيکي از مواد راديواکتيو، در سال 1937 جهت درمان لوسمي در دانشگاه کاليفرنيا در برکلي بود. بعد از آن در 1946 با استفاده از اين مواد توانستند از پیشرفت بیماری در يک بيمار مبتلا به سرطان تيروئيد جلوگيري کنند. البته با توجه به عوارض جانبی این روش، تا سال 1950 کاربرد کلينيکي مواد راديواکتيو گسترش چندانی نیافت، اما سالها بعد دانشمندان دریافتند که ميتوان با هدایت رادیوداروها و تجمع آنها در ارگانِ هدف (مثلا در غده سرطانی) تصاويري از آن تهيه نمود و يا به درمان بافت آسيب ديده کمک کرد. بدین ترتیب در اواسط دهه 60 مطالعات گستردهای در این زمینهها آغاز گشت و در دهه 1970 توانستند با جاروب نمودن و هدایت مواد رادیواکتیو به درون ارگانهای مشخص بدن، از ارگانهاي داخلی بدن مانند کبد و طحال، تومورهاي مغزي و مجاري گوارشي تصاويري را تهيه نمايند. در سالهای دهه 1980 از راديو داروها جهت تشخيص بيماري هاي قلبي استفاده نمودند و هم اکنون نيز با ضريب اطمينان بسيار بالايي از آنها در درمان و تشخيص و پيگيري روند درمان انواع بيماريها استفاده ميگردد.
ساختار رادیو داروها و چگونگی کارکرد آنها
هر رادیو دارو دارای دو جزء است: 1. جزء شیمیایی 2. جزء رادیو ایزوتوپی. رادیوداروها معمولا به صورت خوراکی و یا از طریق تزریق و همچنین استنشاق، به درون بدن وارد میشوند و به روشهای مختلفی که در مقالات بعدی بدانها خواهیم پرداخت، به سوی عضو هدف هدایت میشوند. عضو هدف یعنی آن بخش یا عضوی که دارو باید در آن جمع شده و کارکرد خود را انجام دهد، مثلا یک تومور یا غده سرطانی و یا یکی از اعضای درونی بدن مانند کبد، ریه یا قلب. وقتی که رادیو دارو در عضو هدف جمع میشود بر اساس نوع دارو و کارکرد ویژه آن تا مدت زمان معینی در همان محل باقی مانده و با منتشر کردن پرتو کارکرد و ماموریت خود را انجام میدهد و سپس از طریق فرآیندهای متابولیکی بدن یا از کار میافتد و یا دفع و از بدن خارج میگردد.
انواع کارکردهای رادیو داروها
به طور کلی رادیو داروها دو کارکرد متفاوت دارند که عبارتند از: 1. کارکردهای تشخیصی و 2. کارکردهای درمانی. با این حال فرآیند کلی کارکرد رادیو داروها در هر دو مشابه است و همانگونه که در بخش پیش تشریح شد به طور خلاصه عبارت است از ورود رادیو دارو به درون بدن، هدایت آن به عضو مورد نظر و باقی ماندن رادیو دارو برای یک مدت زمان معین در آن محل و انتشار پرتو از آن.
کارکردهای تشخیصی رادیو داروها
از رادیو داروها به دو روش برای تشخیص بهرهگیری میشود که عبارتند از تشخیص زنده و تشخیص غیر زنده. روشهای تشخیص زنده، آن روشهایی هستند که در آنها یک رادیودارو به درون بدن یک بیمار زنده وارد میگردد. از این رادیو دارو پرتو گاما منتشر میشود و همین پرتوها از بدن عبور کرده و خارج شده و سپس برای تامین اطلاعات مورد نظر از طریق گیرندههای پرتو، دریافت و مونیتور میشوند.
روشهاي تشخیص غير زنده آن کارهايي هستند که بر روي نمونههاي برداشته شده از يک بیمار انجام ميگيردو امروزه به طور گستردهای در آزمایشگاههای پزشکی برای تعیین هورمونها، داروها ، ویروسها و دیگر گونههای آلی در سطح جهان به کار میرود.
کارکردهای درمانی رادیو داروها
کاربردهای درمانی رادیو داروها در مقایسه با کاربردهای تشخیص محدودتر هستند. در این موارد که در بیماران مبتلا به سرطان بسیار از آن بهره برده میشود از پرتوهای منتشر شده از رادیوداروها برای جلوگیری از تقسیم و انتشار سلولهای سرطانی و همچنین ضعیف کردن و نابودسازی آنها استفاده میشود. نابودی سلولهای سرطانی از طریقیونیزاسیون انجام میشود، بنابراین پرتوهایی که دارای یونیزاسیون مخصوص بالا بوده و نیز بردهای کوتاه دارند، برای این عمل مفید هستند، چرا که این رفتار منجر به مقدار زیاد نابودی نسوج در یک منطقه کوچک و محدود میگردد. بهترین ایزوتوپها برای مقاصد درمانی، آنهایی هستند که پرتوهای آلفا یا بتا با انرژی پایین منتشر میکنند.
تزریق رادیو دارو
رادیو دارویی که به مریض تزریق میشود، باید برای مدت طولانی کافی در عنصر هدف بماند، ولی نه طولانیتر از حد ، تا جذب در تشعشع در حداقل باشد. مدت زمانی که در آن دارو مفید است، بستگی به نیم عمر رادیولوژیکی و نیم عمر بیولوژیکی دارد، یعنی مدت زمانی که دارو در بدن میماند، قبل از آنکه بوسیله فرآیندهای متابولیکی از فعالیت افتاده یا از سیستم بدن خارج شود.
نیم عمرهای رادیولوژیکی نوکلوئیدها که معمولا در پزشکی هستهای بکار میروند، به خوبی شناخته شدهاند، ولی رفتار بیولوژیکی و زمان ماندن مولکول که در آن ردیاب وجود دارد، به خوبی مشخص نشده است. این امر یکی از کارهایی است که لازم است داروساز مقادیر این پارمترها را در هنگام آزمایشهای اولیه دارو تشخیص دهد.
نوع تشعشع
نوع تشعشع نشر شده بوسیله رادیونوکلوئید نیز یک فاکتور مهم است که لازم است بررسی گردد. قرار گرفتن نوکلید در محل خاص ، نوع تشعشع مناسب را تعیین میکند. در تشخیص بیشترین استفاده از رادیو داروها در عکسبرداری ساختار بیولوژیکی است. برای عکسها ، جهت تشکیل آنها ، لازم است تشعشع به اندازه کافی برای عبور از میان ماده و رسیدن به آشکارساز با نفوذ باشد. بهتر است تشعشع هنگام عبور حداقل برهمکنش را با ماده بدهد، لذا در تشعشع در حداقل خواهد بود.
بنابراین بهترین رادیونوکلیدها برای روشهای تشخیصی ، آنهایی هستند که تنها اشعه گاما یا اشعه ایکس بدون همراه با تشعشع دیگری منتشر کنند. اینها در ابتدا شامل نوکلوئیدهایی هستند که از طریق جذب الکترون یا گذارهای ایزومری فروپاشی مینمایند.
رفتار رادیونوکلوئیدی که آن را برای عکسبرداری ، مفید میکند، متفاوت از رادیونوکلوئیدی است که برای درمان بکار میرود. در درمانهای تشعشعی ، نکته این است که نسوج مریض نابود شوند.
نابودی نسوج از طریق یونیزاسیون و تولید رادیکال آزاد ایجاد شده بوسیله تشعشع انجام میپذیرد. بنابراین ، تشعشعاتی که دارای یونیزاسیون مخصوص بالا بوده و نیز بردهای کوتاه دارند، برای این عمل مفید هستند، چرا که این رفتار منجر به مقدار زیاد نابودی نسوج در یک منطقه کوچک و محدود میگردد. بهترین نوکلوئیدها برای مقاصد درمانی ، آنهایی هستند که آلفا ، بتاهای با انرژی پایین یا الکترونهای اوژه (Auger) منتشرمیکنند. .
خواص هستهای نوکلوئیدهای شناساگر
قسمت عمده روشهای پزشکی هستهای با بکار بردن چند رادیو نوکلوئید معدود انجام میپذیرد. مثلا بالاتر از 90% ، روشهای تشخیص در مریض ، Tc99m یا ایزوتوپ ید را به عنوان نشان رادیواکتیو مورد استفاده قرار میدهند. عناصری با خواص خوب برای عکسبرداری یا درمان ، لزوما در بیومولکولهای طبیعی رخ نمیدهند، لذا تلاشهای تحقیقاتی زیادی در همراه نمودن این نوکلوئیدها که در ردیابهای مناسبی در مولکولهای آلی حمل کننده هستند، انجام میگیرد. رادیو داروها در شکلهای گوناگون شیمیایی بکار میروند. بعضی از این رادیو داروها به صورت خالص مورد استفاده قرار میگیرند، مانند 133Xe و بعضی به صورت یونی ، 131I ، بسیاری از رادیو نوکلوئیدهای دیگر در داخل مولکولها قرار دارند. این مولکولها از گونههای معدنی کوچک مانند Na332PO4 تا پروتئینهای بزرگ ، مانند آلبومین سرم 125I تشکیل میشوند. حتی در مقیاس بزرگ ، سلولها ممکن است با ردیابهایی چون 51Cr نشان داده شوند.
گرد آورندگان:آقایان نوید کیخسروی،امیررضا اقبالی،رضا بهارلو،اسماعیل دهقان،رضا شاه محمدلو
سامانه ی یکپارچه ی اطلاع رسانی غذا و دارو
اطلاعات مربوط به تهیه داروهای دچار کمبود مقطعی از دروخانه ها در قسمت جستجوی دارو و از طریق تلفن همراه صورت می گیرد. در این سامانه، اطلاعات مربوط به داروهایی که به طور مقطعی دچار کمبود شده اند، از داروخانه های سطح شهر دریافت می شود و از طریق تلفن همراه در اختیار متقاضیان قرار می گیرد. هموطنان با استفاده از این خدمت، در هر منطقه از تهران بزرگ و در هر کجای ایران می توانند داروخانه دارای موجودی از داروی مورد نظر خود را شناسایی (داروخانه ای را که داروی مورد نظر را موجود دارد شناسایی کرده) و سپس جهت تهیه داروی مورد نظر به همان داروخانه مراجعه نمایند.
در قسمت فهرست های دارویی، انواع فهرست های کاربردی جهت استفاده پزشکان و داروسازان عضو سامانه قرار داده شده است که از جمله آنها (از آن جمله می توان به فهرست ... اشاره نمود.) فهرست داروهای تولیدی، وارداتی، شرکتهای پخش دارو (آدرس نشانی و تلفن)، شرکتهای تولیدی دارو (آدرس نشانی و تلفن)، تغییر قیمت داروها و تعهدات بیمه ها و بسیاری اطلاعات کاربردی دیگر قابل مشاهده خواهد بود.
در قسمت اطلاعات عمومی دارویی و مسمومیتها، اطلاعات مورد نظر در سطح مصرف کنندگان دارو(اطلاعاتی جهت استفاده مصرف کنندگان دارو) و بطور کلی گروه غیر پزشکی قرار داده شده است.
در قسمت دریافت بروشورهای دارویی، بروشورهای دارویی بر طبق(مطابق با) اصول و استانداردها و براساس جدیدترین منابع علمی ، جهت استفاده شرکتهای تولیدی و وارداتی قرار داده شده است. بدیهی است، شرکت استفاده کننده می تواند تا حدی که به اصول کلی لطمه وارد نشود، مواردی را بر حسب شرایط ساخت دارو به بروشور اضافه یا کم نماید. این قسمت نیز تنها قابل استفاده توسط شرکتهای دارویی عضو سامانه می باشد.(نیز مانند قسمت فهرست های دارویی، تنها توسط شرکت های دارویی عضو سامانه قابل استفاده می باشد.)
در قسمت (بخش) اخبار، آخرین اخبار دارویی ایران و جهان در اختیار عموم کاربران گذاشته می شود.
منبع:سایت سازمان غذا و دارو
تازهترین رتبهبندی دانشگاههای پزشکی در یک نظام بینالمللی
جديدترين گزارش اسكوپوس درباره شاخص H-Index و میزان استنادات به مقالات علوم پزشکی منتشر شد.
براساس اعلام گروه علم سنجی مرکز توسعه و هماهنگی اطلاعات و انتشارات علمی معاونت تحقیقات و فناوری وزارت بهداشت، علاوه بر شاخص اچ، دانشگاه های علوم پزشکی از نظر تعداد مقالات، تعداد استنادات و تعداد استنادات بدون خود استنادی نيز رتبه بندی شده اند.
در این گزارش، تعداد مقالات، تعداد استنادات و شاخص H دانشگاه های علوم پزشکی اعلام شده است.
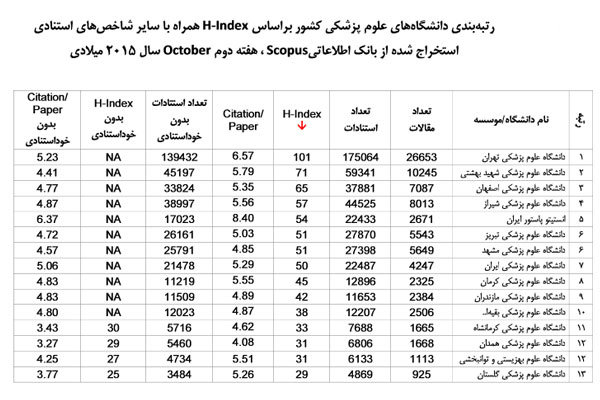
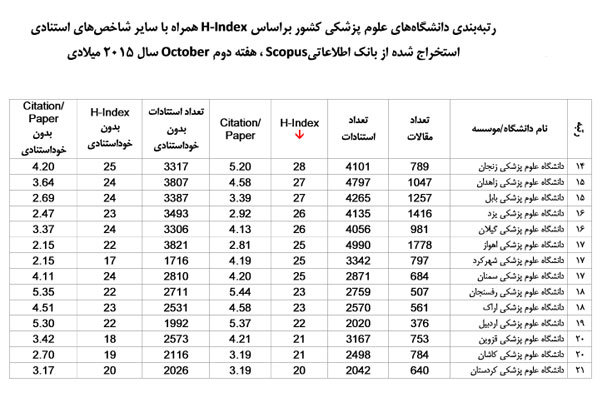
بر اساس این رتبه بندی که هر ۶ ماه یک بار روزآمد و منتشر می شود دانشگاه علوم پزشکی تهران در رتبه نخست قرار گرفته است و تعداد مقالات، تعداد استنادات و شاخص H این دانشگاه به ترتیب بيش از ۲۶ هزار، بيش از ۱۷۵ هزار و ۱۰۱ اعلام شده است.
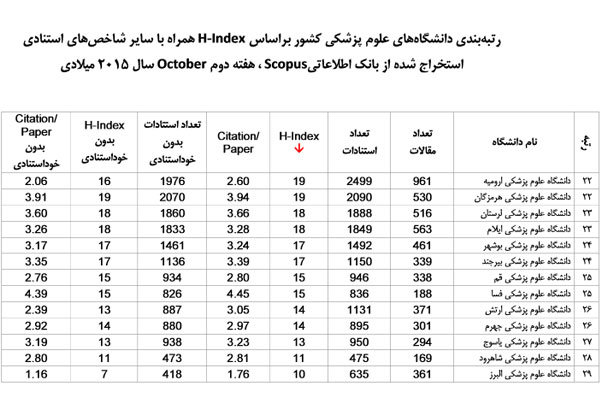
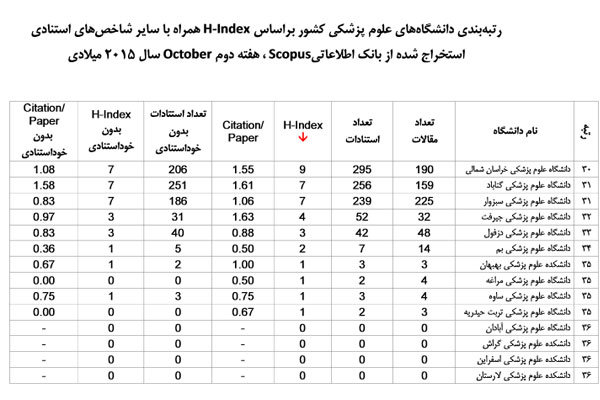
در این گزارش علاوه بر شاخص H-Index، تعداد مقالات، تعداد استنادات، تعداد استناد به ازای مقاله (citation/paper)، تعداد استنادات بدون درنظر گرفتن خود استنادی، شاخص H-Index بدون خود استنادی و نیز شاخص استناد به ازای مقاله بدون خود استنادی محاسبه شده است.
گرایش های تخصصی رشته داروسازی
بر خلاف تصور عامه، داروسازی دارای گرایشهای تخصصی متعددی میباشد كه برگرفته از ماهیت چند بعدی این رشته و ارتباط تنگاتنگ آن با علوم پایه نظیر شیمی، فیزیك، زیست شناسی و علوم بالینی میباشد. دانشجویان علاقهمند میتوانند پس از اتمام دوره عمومی، در یکی از این گرایشها به ادامه تحصیل بپردازند.
1- شیمی دارویی (Pharmaceutical Chemistry):
این رشته تخصصی كه در قالب دورههای آموزشی- پژوهشی منجر به مدرك Ph.D.در سطح دنیا ارائه میشود، از پایهایترین گرایشهای تخصصی داروسازی محسوب میگردد. هدف اصلی در این دوره تربیت متخصصین با دانش قوی شیمی و به ویژه شیمی آلی میباشد، تا با آگاهی از ساختار شیمیایی تركیبات دارویی و گروههای عاملی فعال موجود در ساختمان آنها و با كسب مهارت در زمینه تجزیه و تحلیل واكنشهای شیمیایی تركیبات و ارتباط نوع ساختار شیمیایی آنها با فعالیتهای بیولوژیك بدن انسان، نسبت به طراحی، تركیب، استخراج و شناسایی مواد موثره دارویی اقدام نمایند.
دستیاران این رشته تخصصی در طول تحصیل از توانمندیهای لازم برای كار با ابزارهای پیشرفته آزمایشگاهی و دستگاههای متعدد آنالیز داروها نیز برخوردار میشوند.
2- فارماکوگنوزی (Pharmacognosy):
این رشته تخصصی نیز در قالب دورههای آموزشی–پژوهشی منجر به مدرك Ph.D.در سطح دنیا ارائه میشود.
در این رشته تخصصی، هدف تربیت متخصصین آگاه به خواص مواد موثره دارویی با منشاء طبیعی به ویژه گیاهان دارویی میباشد. كسب دانش لازم در شناسایی گیاهان دارویی، اجزایی از آنها كه دارای خاصیت دارویی میباشد، استخراج و شناسایی مواد موثره موجود در قسمتهای مختلف گیاهان از جمله مهارتهایی است كه فارغالتحصیلان این دوره تخصصی به كسب آنها نایل میشوند. دستیاران این رشته تخصصی در طول تحصیل با گیاهان دارویی بومی (فلور گیاهی) كشورمان و شرایط اقلیمی خاص مورد نیاز برای رشد گونههای خاص آنها كه دارای كیفیت مناسب از نظر تركیب اجزا موثر دارویی میباشند نیز آشنا میشوند.
3- سمشناسی (Toxicology):
این رشته تخصصی از جمله دورههای تخصصی منجر به مدرك Ph.D.میباشد كه علاوه بر فارغالتحصیلان داروسازی، فارغ التحصیلان دورههای كارشناسی ارشد سمشناسی نیز میتوانند در آن ادامه تحصیل دهند. دانشجویان در این دوره ضمن آشنایی با عناصر و تركیبات سمی غیر دارویی كه بشر امروزی در خطر بالقوه و یا بالفعل تماس با آنها قرار دارد، با مسمومیتهای ناشی از ترکیبات دارویی نیز آشنا میگردند. علایم ناشی از تماس تركیبات سمی و یا دوزهای بالای تركیبات دارویی كه میتوانند توسط بیماران یا افراد غیر بیمار به عمد و یا سهواً مصرف شوند و روشهای سمزدایی و درمان حمایتی یا علامتی این نوع مسمومیتها از جمله دانش و مهارتهایی است كه در این دوره تخصصی به دستیاران آموزش داده میشود.
افزون بر اینها، دستیاران این دوره تخصصی با روشهای رایج آزمایشات In vivoو In vitroجهت ارزیابی اثرات و عوارض سمی آنها در سطح سلولی و اندامها، كه از جمله مراحل بسیار مهم در مطالعات فارماكولوژیك پیش از ورود دارو به عرصههای كارآزماییهای بالینی(Clinical Trials) میباشند، آشنا میشوند.
4- داروشناسی (Pharmacology):
این رشته تخصصی (Ph.D.)در ارتباط بسیار تنگاتنگ با رشته سمشناسی میباشد. با این تفاوت كه تمركز عمده آن بر روی بررسی اثرات و عوارض داروها بر اساس مطالعات In vitro و یا In vivoمیباشد. دستیاران در طول این دوره تخصصی با جدیدترین روشهای تعیین دوزهای موثر تركیبات دارویی و مكانیسم اثر آنها و همچنین با روشهای پیشرفته مدلسازی اثرات مورد انتظار داروها در حیوانات، و نیز سطح سلولها و اندامهای هدف آشنا میگردند. فارغالتحصیلان این رشته تخصصی از دانش بسیار بالایی در رابطه با داروها، مكانیسم اثر، عوارض و تداخلات احتمالی اثرات داروهای مختلف برخوردار میباشند.
5- فارماسیوتیكس (Pharmaceutics):
در این رشته تخصصی (Ph.D.)كه در كشور ما با عنوان رشته تخصصی"داروسازی" نیز شناخته میشود، هدف تبدیل مواد موثره دارویی به یك شكل دارویی مناسب و قابل مصرف توسط انسان میباشد، به گونهای كه پس از مصرف دارو توسط بیمار حداكثر مقدار ماده موثره دارویی بتواند در دسترس عضو یا اندام هدف قرار گیرد. آشنایی با روشهای ارزیابی كیفیت فرمولاسیونهای دارویی، سامانههای نوین و پیشرفته دارورسانی، شرایط مناسب نگهداری و بستهبندیهای دارویی و نیز توجه به مدلهای ارزیابی ویژگیهای فارماكوكینتیكی داروها در بدن انسان از جمله مهارتهایی است كه دستیاران این دوره تخصصی به كسب آنها نایل گردیده و میتوانند نقش پویایی در ارتقا كیفی صنعت دارویی كشور ایفا نمایند.
6- داروسازی بالینی (Clinical Pharmacy):
این رشته تخصصی یكی از رشتههای نوپا در كشور ما میباشد كه با توجه به ماهیت بالینی این گرایش، دوره آموزش آن به صورت دوره تخصصی بالینی مشابه دستیاران تخصصی رشته پزشكی طراحی گردیده است. البته بر خلاف دورههای دستیاری پزشكی، دستیاران داروسازی بالینی میبایست یك سری دروس مرتبط با پزشكی نظیر فیزیوپاتولوژی، فارماکواپیدمیولوژی، سمشناسی بالینی، فارماکوکینتیک بالینی و... را در قالب یک دوره 5/1 تا 2 ساله پیش از حضور در بخشهای بالینی مراكز بیمارستانی بگذرانند. هدف این دورهتخصصی تربیت متخصصین مسلح به اطلاعات كاربردی داروها كه مهارت لازم برای ارائه خدمات و مراقبتهای دارویی (Pharmaceutical care) در مراكز بیمارستانی و بخشهای بالینی را دارا هستند، میباشد. فارغالتحصیلان این دوره مشاورانی مطمئن برای پزشكان و اعضای تیم درمان و نیز بیماران میباشند.
دستیاران این دوره تخصصی مهارتهای لازم برای برقراری ارتباط موثر با بیمار و تیم درمان، پایش اثرات و عوارض داروها در بیماران، شناخت تداخلات رایج و مهم دارویی شامل تداخلات دارو –دارو، دارو –غذا و دارو–بیماری، راههای پیشگیری یا كنترل آنها و همچنین روشهای تنظیم دوزهای مناسب دارویی را در طول دوره تحصیل خود كسب مینمایند.
7- بیوتكنولوژی دارویی (Pharmaceutical Biotechnology):
این رشته تخصصی (Ph.D.)نیز از جمله دورههای تخصصی نوپا در كشور ما میباشد. اگر چه موضوعات مورد توجه در این دوره تخصصی قبلاً در بطن سایر گرایشهای تخصصی داروسازی مورد عنایت بوده است، ولی با توجه به پیشرفت سریع آن به ویژه در دهه 1980 و 1990 میلادی، امروزه به عنوان یكی از برجستهترین رشتههای تخصصی داروسازی كه نیازمند فنآوری پیچیده و پیشرفتهای میباشد، مطرح است. در این دوره تخصصی هدف كسب دانش و مهارت لازم برای بهرهبرداری از علوم سلولی- مولكولی، میكروبیولوژی و ژنتیك جهت ساخت و تولید انبوه مواد موثره دارویی میباشد. بهرهبرداری از میكروارگانیسمهایی نظیر باكتریها و قارچها به عنوان كارخانجات طبیعی تولیدداروها و یا به كارگیری میكروارگانیسمها در مهار و كنترل بیماریها از جمله مباحث مورد توجه در این رشته تخصصی میباشند.
8- داروسازی هستهای یا رادیوفارماسی (Nuclear Pharmacy):
این دوره تخصصی (Ph.D.) در حال حاضر توسط دانشكده داروسازی تهران و با همكاری سازمان انرژی اتمی و اخیراً توسط دانشكده داروسازی ساری، برگزار میشود. در طی این دوره دستیاران با رادیوداروها، روشهای شناسایی (Detect)و سنجش آنها، روش تولید رادیوداروها (Labling)و كاربرد رادیوداروها در تشخیص، درمان و یا پیشگیری از بیماریها آشنا شده و مهارتهای مرتبط با به كارگیری و كار با آنها را كسب مینمایند. به لحاظ ماهیت خاص این دوره تخصصی، دانشجویان با تكنولوژیهای پیشرفته مربوط به بكارگیری و تماس با رادیوایزوتوپها آشنا میشوند.
9- اقتصاد و مدیریت دارو (Pharmaceutical Administration and Pharmacoeconomics):
این دوره تخصصی (Ph.D.)كه با همت اساتید دانشكده داروسازی شهید بهشتی راهاندازی گردید، در حال حاضر تنها توسط این دانشكده و دانشكده داروسازی تهران ارائه میشود. رسالت این رشته، تربیت متخصصین كارآمد با توانمندیهای مدیریتی در شناسایی و حل مشكلات نظام دارویی كشور و ارتقاء سطح ارائه خدمات نظام سلامت با مدیریت صحیح منابع مالی در دسترس میباشد. در طی این دوره، دانشجو با مباحث مختلف مربوط به اقتصاد داروئی و مدیریت مالی و سایر مباحث مرتبط با رشته آشنا خواهد شد.
علاوه بر تخصصهای فوقالذكر كه در كشور ما دایر میباشند، با توجه به پیشرفت شگرفی كه علم داروسازی در سطح جهان با آن روبروست، گرایشهای تخصصی جدیدتری نیز راهاندازی و در حال اجرا میباشند كه از جمله آنها میتوان به فارماكواپیدمیولوژی، فارماكوژنتیك، ایمونوفارماكولوژی و مدیریت دارویی ( Pharmaceutical management)اشاره كرد.
آزمون دورههای پذیرش دستیار رشتههای مختلف داروسازی معمولاً در تیرماه هر سال برگزار گشته و قبول شدگان از مهرماه همان سال دوره خود را شروع مینمایند. (تا پیش از سال 1385 این آزمون در اسفندماه برگزار میشد). شرایط عمومی و اختصاصی شركت در این آزمونها نیز همه ساله چند ماه پیش از برگزاری آزمون از طریق دبیرخانه شورای آموزش داروسازی و تخصصی اعلام میگردد.
آزمون دستیاری از دو بخش امتحان كتبی و مصاحبه تشكیل میشود كه به ترتیب 80% و 20% امتیاز آزمون از این دو بخش كسب میگردد. در بخش مصاحبه به معدل دوره عمومی، تناسب پایاننامه دوره عمومی با دوره تخصصی انتخاب شده، تعداد مقالات یا احتمالاً مشاركت در تألیف و ترجمه كتب، سطح زبان انگلیسی (و یا آشنایی با سایر زبانهای رایج بینالمللی)، فعالیتهای فوق برنامه در طول دوران دانشجویی یا سایر خصوصیات برجسته فردی و نیز میزان علاقه و انگیزه داوطلب برای ادامه تحصیل توجه میشود.
10- نانوفناوری دارویی (Pharmaceutical Nanotechnology):
این رشته (Ph.D.)نیز كه به تازگی در كشور راهاندازی شده است، با هدف تربیت متخصصین كارآمد در عرصه نانوفناوری دارویی در راستای خودكفایی كشور در تولید محصولات نانوزیست فناوری و اشتغال آنها در مراكز علمی و دانشگاهی كشور، مراكز تحقیقاتی پزشكی – دارویی و صنایع داروئی طراحی شده است. در طول این دوره دانشجو با مباحث گوناگونی نظیر بیولوژی سلولی مولكولی پیشرفته، نانوبیو مواد، كشت سلول و بافت، Nanomedicine، فارماكوكینتیك پیشرفته، ژن درمانیو... آشنا خواهد شد.
11- كنترل دارو (Control of Pharmaceuticals):
این رشته (Ph.D.)كه به تازگی در كشور راهاندازی شده است، با هدف تربیت متخصصین كارامد در زمینه كنترل كیفیت انواع مواد اولیه و فرآوردههای دارویی و همچنین بهداشتی – آرایشی، جهت ارائه خدمت در صنایع داروسازی و بهداشتی – آرایشی، آزمایشگاههای كنترل كیفیت فرآوردههای دارویی سراسر كشور و همچنین مراكز تحقیقاتی كشور، طراحی شده است. در طی این دوره مباحث گوناگونی شامل كنترل میكروبی داروها، كنترل كیفیت زیست داروها، ایمنی دارو، كنترل فیزیكوشیمیایی پیشرفته مواد و فرآوردههای دارویی، طراحی و معتبرسازی روشها و تجهیزات آنالیز، كینتیك شیمیایی و پایداری مواد و فراوردههای دارویی و همچنین كنترل و تضمین كیفیت مواد و فرآوردههای دارویی به دانشجویان آموزش داده میشود. منبع:سایت دانشکده ی داروسازی شهید بهشتی
اثرات زیست محیطی اشعه ایکس
همواره این امکان وجود دارد که به هر دلیلی یکی از الکترون های موجود در اتم از لایه
مربوطه جدا شود. چنانچه این الکترون از میدان کولنی هسته کاملاً خارج شود، می گوییم اتم
یونیزه شده است، که در این حالت یک یون مثبت و یک الکترون آزاد خواهیم داشت.
چنانچه الکترون جدا شده از لایه، کماکان در میدان کولنی هسته باقی بماند در این صورت
فقط یک جابجایی الکترون با کسب انرژی از لایه پایین تر به لایه بالاتر انجام شده است که
الکترون بلافاصله با آزاد نمودن آن انرژی به لایه خود باز می گردد. در این حالت میگوییم که
اتم برانگیخته و یا تهییج شده است. طبیعی است بیشترین انتقال انرژی به ماده از طریق
یونش خواهد بود
گرد آورنگان:خانم ها زهرا سنجری ، فاطمه حسن نژاد ، رضوان اصغرنژاد
IsoRay’s Cesium-131
IsoRay’s Cesium-131 Isotope Produces Excellent Results in Treating Metastatic Brain Cancer as Published in the Journal of Neurosurgery
100% Local (Resection Cavity) Freedom From Progression With 19.3 Month Median Follow-Up
Richland, WA (August 5, 2014) – – IsoRay Inc. (NYSE MKT: ISR), a medical technology company and innovator in seed brachytherapy and medical radioisotope applications, today announced the publication of the first major peer reviewed study showing superior results using IsoRay’s Cesium-131 seeds in the treatment of metastatic brain cancer.
Powered by:ladies Shokoofe Karimpour ,Fateme Moridi ,Maryam Shokri
فلوئورسانس
فلوروسانس
نورتابناکی
نورتابناکی یا فتولومینسانس (Photoluminescence) فرایندی است که طی آن ماده فوتون را جذب کرده و سپس بازتاب میدهد.
در این روش نحوه تحریک بلور جامد از طریق جذب فوتونی است. در تجربه دیده میشود که طول موج جذب و انتشار عملا کمی فرق دارند و انرژی انتشار به مراتب کمتر(فرکانس پایین تر)است. این انتقال فرکانسی اصطلاحا انتقال استوکس نیز نامیده میشود.
گرد آورندگان: خانم ها فاطمه صادقی، نادیا غلامی، زهرا گلمرادی
گاما دردرمان
گاما دردرمان
مقدمه
گاما پرتویی الکترومغناطیسی با بسامد بالا و در نتیجه انرژی بالاست. کاربرد اشعه ی ایکس از گاما بیش تر است. اشعهٔ گاما پرتویی یونی و در نتیجه برای سلامتی مضر است. پرتو گاما بطور معمول در نتیجهٔ فروپاشی حالتهای انرژی بالای هستههای اتم تولید میشود، اما روشهای دیگری نیز برای تولید آن وجود دارد. پل ویلارد دانشمند فرانسوی در سال ۱۹۰۰ در حین مطالعهٔ رادیوم موفق به کشف اشعهٔ گاما شد طول موج پرتو گاما بسیار کوتاه بوده و از 01/0 تا 1 آنگستروم تغییر میکند. جرم آن در مقیاس اتمی صفر، سرعت آن برابر سرعت نور و بار الکتریکی آن صفر است. انرژی پرتو گاما از ۱۰ کیلو الکترون ولت تا ۱۰ مگا الکترون ولت تغییر میکند. برد پرتو گاما بسیار زیاد، مثلاً در هوا چندین متر میباشد. خاصیت ایجاد یونیزاسیون و برانگیختگی در پرتو گاما نیز وجود داشته ولی به مراتب کمتر از ذرات آلفا و بتا میباشد. مثلاً اگر قدرت یونیزاسیون متوسط پرتو گاما را یک فرض کنیم، قدرت یونیزاسیون متوسط ذره بتا ۱۰۰ و ذره آلفا ۱۰۴ خواهد بود. قدرت نفوذ این پرتو به مراتب بیشتر از ذرات بتا و آلفا است. طیف انرژی پرتو گاما، همانند ذرات آلفا تک انرژی است، یعنی تمام فوتونهای گامای حاصل از یک عنصر رادیواکتیو دارای انرژی یکسانی هستند. این پرتو از لحاظ انرژی شباهت بسیاری با پرتو ایکس دارد، ولی مهمترین تفاوت این پرتو با پرتو ایکس در این است که اولاً منشأ تولید پرتو ایکس یک واکنش اتمی است، در حالی که منشأ تولید پرتو گاما یک برهمکنش هستهای است و دوم اینکه طیف پرتو گاما نسبت به پرتو ایکس متمرکزتر میباشد.از آنجا که عناصر تولید کننده پرتو گاما، فراورده فرعی تجزیه اتمی بوده و یا جزء ضایعات اتمی محسوب میشوند، استفاده از پرتو مذکور جزء ارزانترین روشهای نگهداری مواد غذایی است.
گرد آورنذگان:خانم ها زهرا نیکنام،نگار گودرزی،ریحانه شجاعی
رادیو دارو ها
رادیو دارو چیست؟
در یک تعریف ساده به هر دارویی که در ساختار آن یک رادیو ایزوتوپ موجود باشد رادیودارو گفته میشود، رادیوایزوتوپها در واقع عناصر ناپایداری هستند که با توجه به ساختار اتمیشان از خود پرتو (Radiation) منتشر میکنند. این پرتوها که شامل پرتوهای آلفا (α)، بتا (β) و گاما (γ) هستند دارای طول موج و سطح انرژی متفاوتی هستند و بر همین اساس میتوانند در فرآیندهای مختلف تشخیصی و درمانی به کار گرفته شوند. سودمندترین رادیو ایزوتوپها در پزشکی هستهای رادیوایزوتوپهای تابش کننده پرتو گاما هستند، زیرا پرتوهایی که از این مواد در درونِ بدن تابش میشوند را میتوان از بیرون بدن به سادگی تشخیص داد.
گرد آورندگان:آقایان نوید کیخسروی،امیررضا اقبالی،رضا بهارلو،اسماعیل دهقان،رضا شاه محمدلو
سامانه ی یکپارچه ی اطلاع رسانی غذا و دارو
اطلاعات مربوط به تهیه داروهای دچار کمبود مقطعی از دروخانه ها در قسمت جستجوی دارو و از طریق تلفن همراه صورت می گیرد. در این سامانه، اطلاعات مربوط به داروهایی که به طور مقطعی دچار کمبود شده اند، از داروخانه های سطح شهر دریافت می شود و از طریق تلفن همراه در اختیار متقاضیان قرار می گیرد. هموطنان با استفاده از این خدمت، در هر منطقه از تهران بزرگ و در هر کجای ایران می توانند داروخانه دارای موجودی از داروی مورد نظر خود را شناسایی (داروخانه ای را که داروی مورد نظر را موجود دارد شناسایی کرده) و سپس جهت تهیه داروی مورد نظر به همان داروخانه مراجعه نمایند.
منبع:سایت سازمان غذا و دارو
گرایش های تخصصی رشته داروسازی
بر خلاف تصور عامه، داروسازی دارای گرایشهای تخصصی متعددی میباشد كه برگرفته از ماهیت چند بعدی این رشته و ارتباط تنگاتنگ آن با علوم پایه نظیر شیمی، فیزیك، زیست شناسی و علوم بالینی میباشد. دانشجویان علاقهمند میتوانند پس از اتمام دوره عمومی، در یکی از این گرایشها به ادامه تحصیل بپردازند.
منبع:سایت دانشکده ی داروسازی شهید بهشتی
